| Strain Name |
NOD.CB17-PrkdcscidIl2rgtm1/Bcgen |
Common Name |
B-NDG mice |
| Background |
NOD-scid |
Catalog number | 110586 |
|
Related Genes |
Male: Prkdc (-/-), Il2rg (X-/Y); Female: Prkdc (-/-), Il2rg (X-/X-) |
||
背景概述
B-NDG®小鼠(NOD.CB17-PrkdcscidIl2rgtm1/Bcgen)是百奥赛图公司自主开发的,NOD-scid遗传背景的Il2rg基因敲除小鼠,缺乏成熟的T、B和NK细胞,是目前国际公认的免疫缺陷程度高、非常适合人源细胞或组织移植的工具小鼠。
• NOD(non-obese diabetes)遗传背景:自发I型糖尿病;其巨噬细胞对人源细胞吞噬作用弱;先天免疫系统,如补体系统和树突状细胞功能降低。
• Prkdc null(DNAPK,scid):Prkdc(protein kinase DNA-activated catalytic)基因突变,小鼠的功能性T和B细胞缺失,淋巴细胞减少,表现为细胞免疫和体液免疫的重度联合免疫缺陷(severe combined immunedeficiency, scid)。
• Il2rg null:Interleukin-2受体的gamma链(IL-2R γc,又称CD132)位于小鼠X染色体上,是具有重要免疫功能的细胞因子IL2、IL-4、IL-7、IL-9、IL-15和IL-21的共同受体亚基,该基因敲除后的小鼠机体免疫功能严重降低,尤其是NK细胞的活性几乎丧失。
B-NDG®小鼠:综合了NOD-scid-Il2rg null背景特征,具有重度免疫缺陷表型,无成熟T细胞、B细胞和功能性NK细胞,细胞因子信号传递能力缺失等。非常适合人造血干细胞及外周血单核细胞的移植和生长。
B-NDG 小鼠优势
• 世界公认的重度免疫缺陷小鼠
• 与NOD-scid小鼠相比寿命更长,平均长达1.5年
• 对人源细胞和组织几乎没有排斥反应
• 少量细胞即可成瘤,依赖于细胞系或细胞类型
• 无B淋巴细胞泄漏
主要应用领域
• 人源细胞或组织移植
• 肿瘤和肿瘤干细胞研究
• ES和iPS细胞研究
• 造血和免疫学研究
• 人类疾病感染模型研究
• 新的人源化动物模型研发
B-NDG商标申请
百奥赛图(北京)生物医药科技股份有限公司分别对“B-NDG”进行了第5类、第31类、第42类和第44类进行了商标申请。各字母代表含义:B-Biocytogen; N-NOD background; D- DNAPK(Prkdc) null; G- G: IL2rg knockout。
第5类:人用药;医用水蛭;医用生物标志物诊断试剂;医用或兽医用微生物培养物;医用营养食物;净化剂;兽医用制剂;杀虫剂;医用填料;兽医用干细胞(截止)
第31类:活动物;活家禽;活鱼;甲壳动物(活的);树木;谷(谷类);植物;植物种子;动物栖息用干草;饲料(截止)
第42类:质量控制;化学研究;生物学研究;临床试验;材料测试(截止)
第44类:医药咨询;医院;人工授精;饮食营养指导;动物养殖;兽医辅助;人工授精(替动物);试管授精(替动物);卫生设备出租;试管授精(截止)

小鼠饲养注意事项
B-NDG®小鼠饲养环境需要注意哪些问题?
百奥赛图的B-NDG®小鼠都是在隔离软包中饲养繁殖的,没有在IVC环境繁殖过,根据我们公司的经验,在严格水平的IVC环境(SPF级别)饲养时,可以保证小鼠2个月的健康存活时间,并能满足多数的实验项目要求;
但是鉴于国内动物房管理及微生物水平参差不齐,我们不能保证在所有IVC环境下一定都能健康饲养,建议一定要尽量提高现有IVC动物房的洁净标准,如饲养笼具和垫料都要经过高压灭菌或Co60辐照,并保证一周更换1次,操作要在无菌操作台进行等。越干净的环境越能保证小鼠更长时间的健康生长!
B-NDG®小鼠饲养中注意事项
饲料
百奥赛图繁殖生产使用的是美国Labdiet公司的专用饲料5CJL,蛋白含量19.3%,脂肪含量6.2%,并且维生素K含量达到20ppm(高压前),采用的灭菌方式是Co60辐照灭菌,可以保证小鼠的健康生长繁殖
如果是国内饲养B-NDG®小鼠用于实验,不进行繁殖,也可用国内饲料,我们建议使用科奥协力的饲料“SPF大小鼠生长繁殖饲料”,蛋白含量22.7%,脂肪含量4.7%,且已经过Co60照射,在SPF级别(IVC环境)下饲养,也可以健康生长至少2个月。
注:推荐使用美国Labdiet公司的专用饲料5CJL。
饮水
百奥赛图是在隔离器中饲养,符合高级别的无病原体环境,采用的是高压后的纯水作为饮用水。
如果其他实验室要在普通SPF级别饲养,建议按照Jackson Lab的标准,采用酸化水(用HCl调节PH至2.5-3.0),之后再高压灭菌,可有效预防假单胞菌和金黄色葡萄球菌的污染,也可采用纯水直接灭菌,但一定要及时更换饮用水及水瓶,在饲养过程中,无论水瓶中的水是否饮用完,应当每3天更换一次新的水瓶。
垫料
建议垫料使用刨花垫料,材质柔软蓬松、吸湿性强、无尘、无杂质、无异味,经过高压或者辐照灭菌处理。
垫料每周更换一次,如不在隔离包饲养,需要在超净工作台更换垫料,而且需要使用消毒过的镊子转移小鼠到新的笼盒,避免用手直接接触小鼠。
环境
在饲养过程中,保证足够的光照强度(太强或太弱都不行)和光照时间,一般采用12小时光照,12小时黑暗的饲养模式。
环境温度保持在20-26℃,日温差不超过4℃。
饲养笼盒材质要无毒无害,便于清洁和消毒。每周至少要清洗消毒一次

运输
百奥赛图B-NDG®小鼠的运输可以采用陆运和空运两种方式,运输过程中我们尽量保证轻拿轻放避免小鼠在途中颠簸。但小鼠在运输过程中依然可能会有应激反应,加速小鼠的代谢和排泄,小鼠有可能出现不同程度的脱水状况导致体重减轻。尽管我们在运输箱内添加了果冻供动物采食,但长途运输应激仍会使一些小鼠出现体重减轻现象。一般运输所造成的小鼠体重消耗为10%左右,如果运输时间长、路途远、装箱密度大,体重消耗可能达到15%。不过这种情况一般经过7-15天的适应性饲养(建议使用Labdiet饲料),大部分体重便可恢复(不能100%同步恢复)。
适应性饲养
1)为什么要进行适应性饲养?
所谓适应性饲养,是指实验动物由繁殖地转移到实验动物房以后,在实验之前,为了使之适应环境而喂养几天的过程。因为运输、转移过程中,动物会有应激反应,为消除应激反应,一般需要为期7-15天的适应性饲养。
2)适应性饲养过程中注意哪些问题?
配置好饲养的条件,按照第1.10.1所规定。努力使之在“新家”舒服地过日子。密切观察其毛发、排泄物、活动情况,这是考察动物是否有疾病的外在表现。注意与实验室原有饲养的动物隔开一定的距离,其它动物的声音、排泄的氨会对新来的动物有一定的影响。适应性饲养是保证实验成功的前提之一。
表型分析
小鼠生长曲线
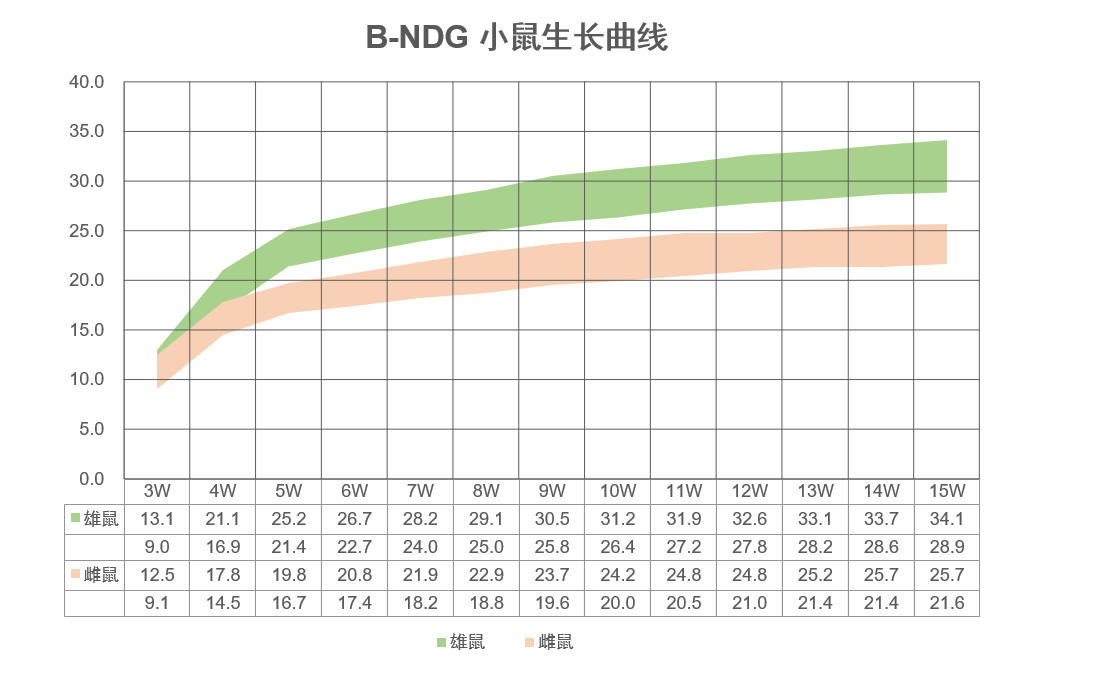
图1. B-NDG小鼠生长曲线
雌雄小鼠各50只,小鼠3周龄断奶后(出生日期±3天)每周固定日期进行称重,数据收集共13周。
小鼠血清抗体检测
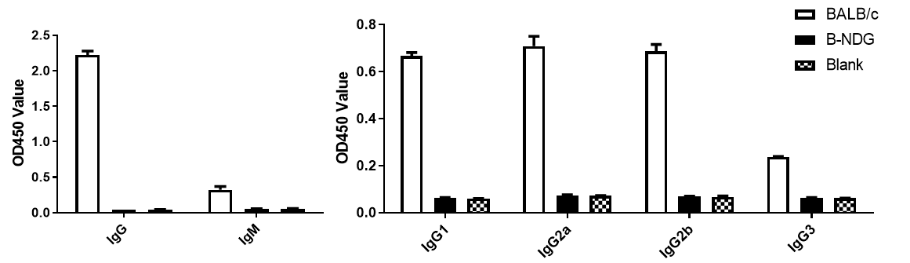
图2. B-NDG®小鼠血清抗体亚类检测
(A)空白对照及B-NDG小鼠OD值均在0.04左右,BALB/c小鼠OD值显著高于B-NDG 小鼠,可认为B-NDG 小鼠血清中无IgG和IgM存在。(B)空白对照孔OD450均在0.06左右,本底值低于0.1,说明捕获抗体、酶标抗体和BSA之间没有交叉反应。分别检测BALB/c小鼠和B-NDG 小鼠血清IgG1、IgG2a、IgG2b和IgG3,BALB/c小鼠体内存在IgG各亚类抗体,B-NDG小鼠血清中不存在IgG各亚类抗体(n=3)。
结果表明:B-NDG小鼠作为缺失T细胞、B细胞的重度免疫缺陷模式小鼠,体内不存在任何类型的Ig抗体。
T细胞、B细胞和NK细胞的检测
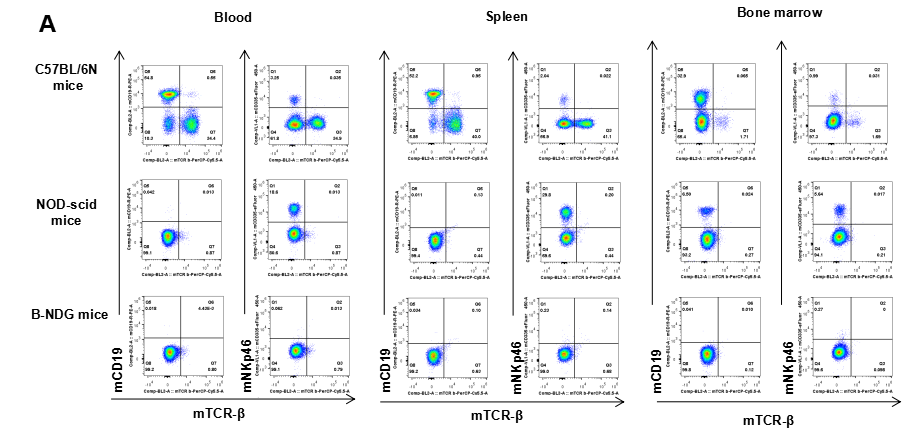
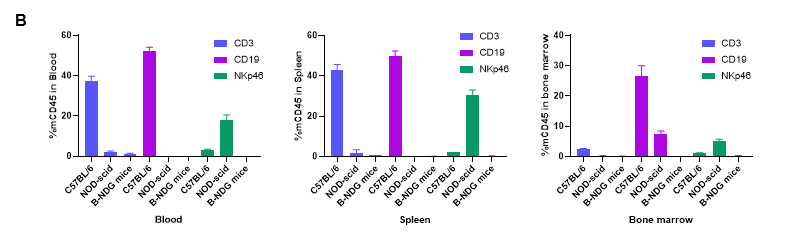
图3. B-NDG小鼠的T 、B和NK细胞的完全缺失
从 C57BL/6N、NOD-scid 和B-NDG小鼠(n=3,6 周龄,雌性)中分离血细胞,脾细胞,骨髓。对其进行流式细胞术分析,以评估白细胞亚群。 (A) 代表性流式图。 (B) FACS 分析结果,在 C57BL/6N 小鼠中可检测到 T 细胞、B 细胞和 NK 细胞,在NOD-scid小鼠中可检测到NK细胞,但在 B-NDG 小鼠中均未检测到。
髓系细胞免疫分型
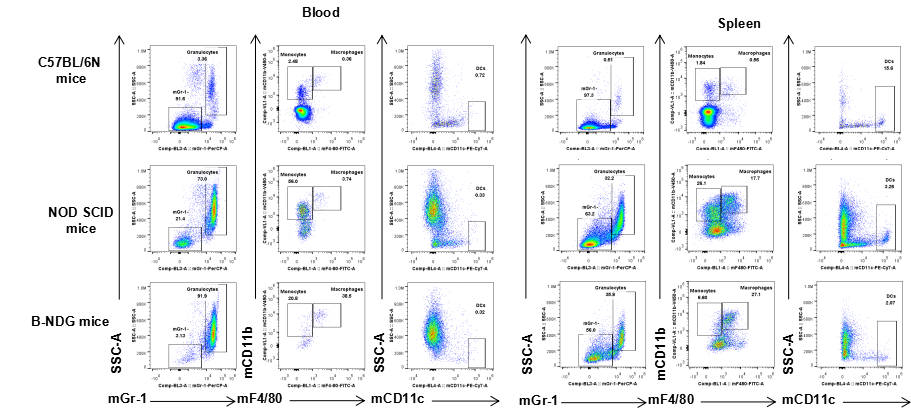
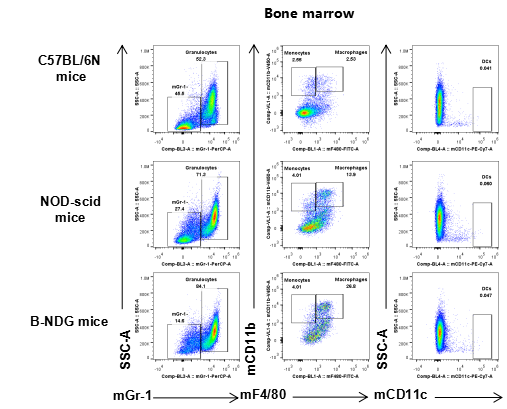
图4. B-NDG小鼠的髓系细胞分型
从 C57BL/6N、NOD-scid 和B-NDG小鼠(n=3,6 周龄,雌性)中分离血细胞,脾细胞,骨髓。对其进行流式细胞术分析,以评估髓系细胞亚群。结果显示,在B-NDG小鼠中可检测到髓系细胞。
Granulocytes :mCD45+mGr-1+, DCs:mCD45+mCD11c+, Macrophages:mCD45+mCD11b+mF4/80+,
Monocytes: mCD45+mCD11b+mF4/80-.
B-NDG脾脏组织学检测
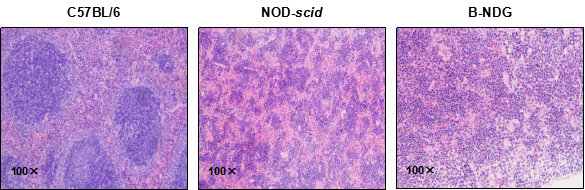
图5.小鼠脾脏组织切片及HE染色
取C57BL/6、NOD-scid 和 B-NDG小鼠(n = 3,9 周龄,雌性)脾脏,对脾脏样本进行组织切片及HE染色。结果显示:C57BL/6 小鼠脾脏结构正常,滤泡清晰。NOD-scid 小鼠的脾脏显示白髓发育不全。B-NDG 小鼠的脾脏显示滤泡结构完全丧失。
B-NDG脾脏组织学检测
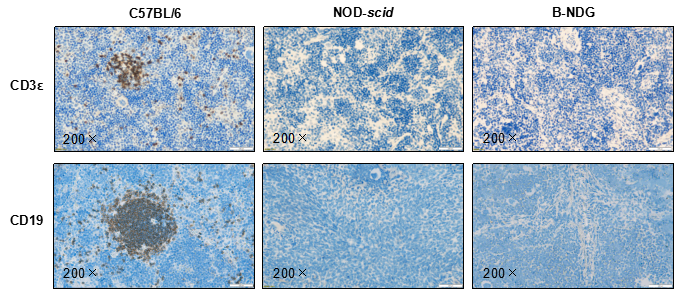
图6.小鼠脾脏组织切片及IHC染色
取C57BL/6、NOD-scid 和 B-NDG小鼠(n = 3,9 周龄,雌性)脾脏,对脾脏样本进行组织切片及IHC染色。结果显示:C57BL/6 小鼠脾脏 CD3ε 和 CD19 表达正常(棕色),小鼠 B-NDG 小鼠无 CD3ε 和 CD19 表达。
血常规检测
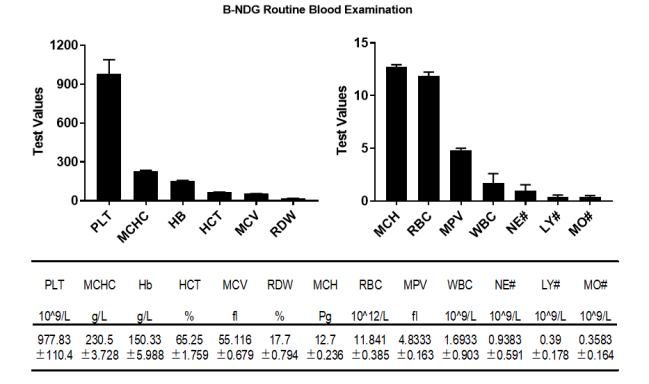
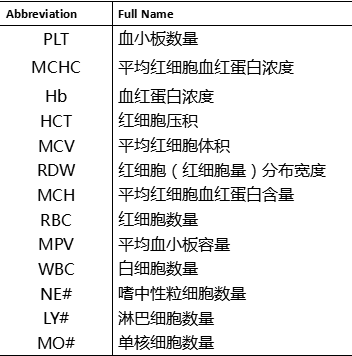
图 7. B-NDG 小鼠的全血细胞计数 (CBC)
试验采集 B-NDG 小鼠(n = 6,6 周龄,雌)的血液并分析 CBC。数值表示为平均值±SEM。
血生化检测
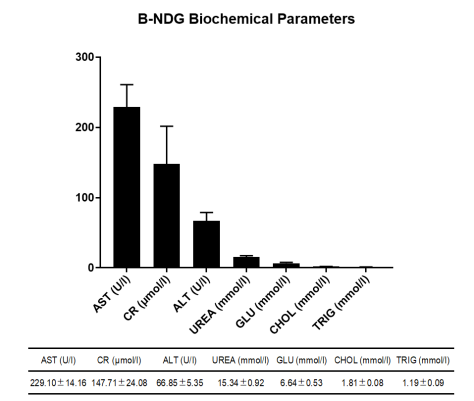
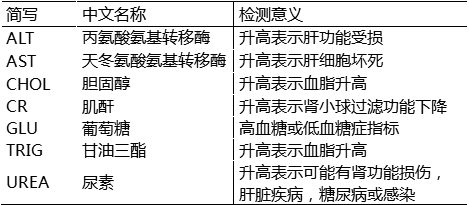
图 8. B-NDG 小鼠血液生化检测结果 。
采集 B-NDG 小鼠(n = 6,6 周龄,雌)的血清,并分析 ALT、AST、CHOL、CR、GLU、TRIG 和 UREA 的水平。数值表示为平均值±SEM。仪器:Thermo Fisher scientific#Indiko
CDX 肿瘤模型及药效评价
CDX 淋巴癌转移模型
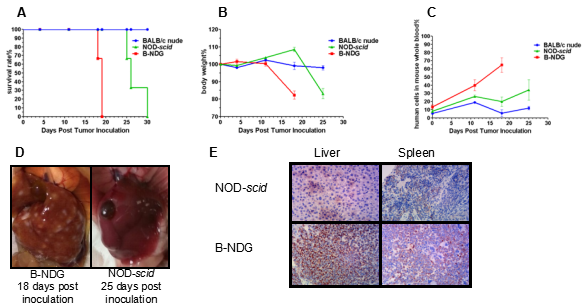
图9. Raji淋巴肿瘤细胞在B-NDG®小鼠上能更有效地建立系统和转移肿瘤模型。
对B-NDG®、NOD-scid、BALB/c Nude小鼠通过尾静脉注射相同数量(5 × 105)的Raji细胞,后在不同的时间点记录并分析小鼠的如下各种指标。
A.细胞接种后记录小鼠生存情况,绘制Kaplan-Merier生存曲线。
B.细胞接种后每周小鼠体重变化(g),并计算出相对于接种当天的相对体重。
C.小鼠外周血中人源细胞百分率变化。接种Raji细胞后,每周通过眼眶静脉丛采取100 μl全血,提取DNA,通过q-PCR技术检测小鼠外周血中人源细胞比率。
D.接种Raji细胞后小鼠肝脏对比。接种后待小鼠体重下降超过30%后执行安乐死并解剖脏器,进行拍照。
E.接种Raji细胞后小鼠脏器免疫组化染色。一抗为鼠抗人线粒体膜蛋白抗体。
B-NDG®小鼠 CDX淋巴癌体内药效实验
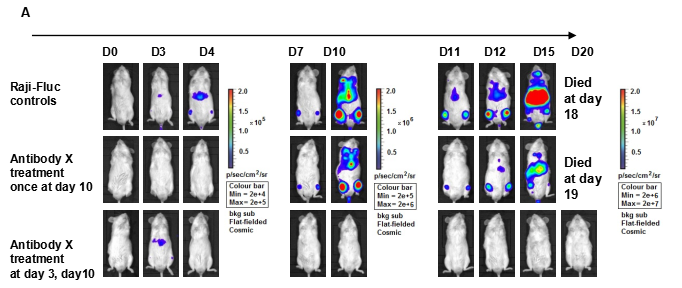
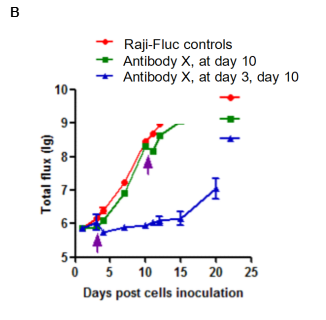
图10. 基于B-NDG小鼠的Raji淋巴癌转移模型及药效评价
对B-NDG®小鼠通过尾静脉注射相同数量(5×105)的Raji-Fluc细胞,并在第3天以及第10天尾静脉注射相同计量的抗体X,之后在不同的时间点成像观察肿瘤生长状况。A.不同时间点对小鼠成像观察肿瘤生长情况;B.不同分组小鼠成像下肿瘤细胞荧光强度曲线。结果表明,早期治疗(Raji细胞移植3天,10天)的治疗效果显著,晚期治疗(Raji细胞移植10天)的治疗效果明显变差,基本无效。
B-NDG®小鼠进行抗人CD47抗体药效验证实验
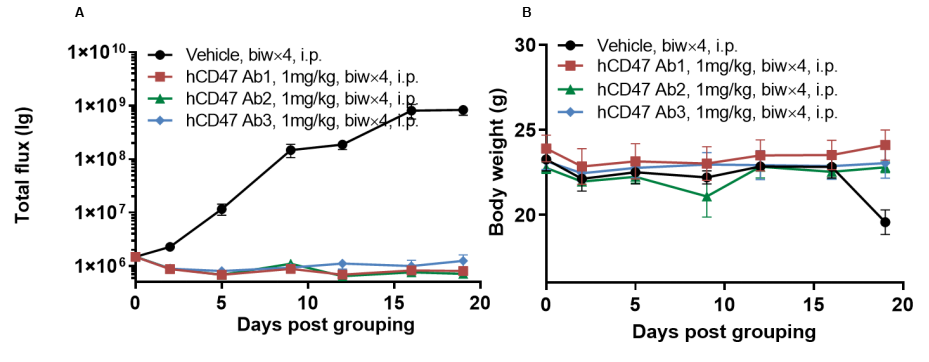
图11.利用B-NDG®小鼠进行抗人CD47抗体药效验证实验
图10.抗人CD47抗体在B-NDG小鼠中的抗肿瘤活性。
将人B-荧光素酶-GFP Raji细胞(B淋巴细胞)尾静脉植入B-NDG。当荧光强度达到约1.0E + 06(n = 6)时,将小鼠分组,此时用抗人CD47抗体处理,剂量和时间表如图A所示。(A)荧光成像仪用于监测小鼠中的肿瘤荧光。(B)给药期间的体重变化。结果表明,3种抗体对B-NDG小鼠的肿瘤生长抑制有效。B-NDG是人CD47抗体有效性研究的有力模型。数值表示为平均值±SEM。
B-NDG®小鼠进行CAR-T药效验证实验
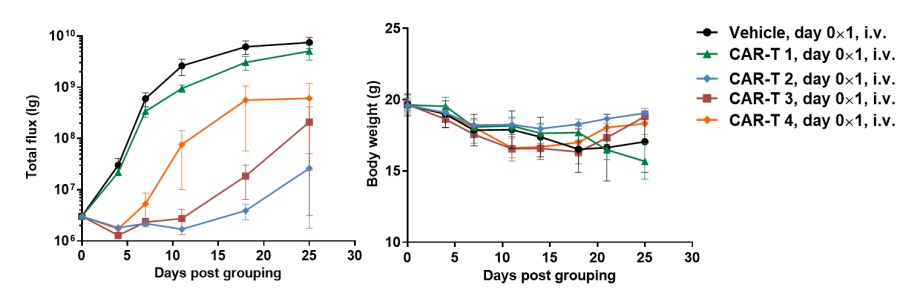
图 12.CAR-T 疗法在 B-NDG 小鼠中的抗肿瘤活性。
将B-luciferase-GFP Raji cells (B lymphocytes)尾静脉植入 B-NDG小鼠。当荧光强度达到约 1E + 06 (n = 6) 时,将小鼠分组,用CAR-T 细胞 (1E + 07) 处理。(A) Raji-Luciferase 细胞系经不同 CAR-T 细胞处理后的信号强度;(B) 处理期间的体重变化。结果显示,4 种 CAR-T 细胞在 B-NDG 小鼠中表现出不同地抑制肿瘤生长活性。结果表明:B-NDG 小鼠可以作为 CAR-T 细胞治疗研究的有力模型。数值表示为平均值±SEM。
人免疫系统重建模型及药效评价
利用B-NDG 小鼠进行PBMCs免疫重建
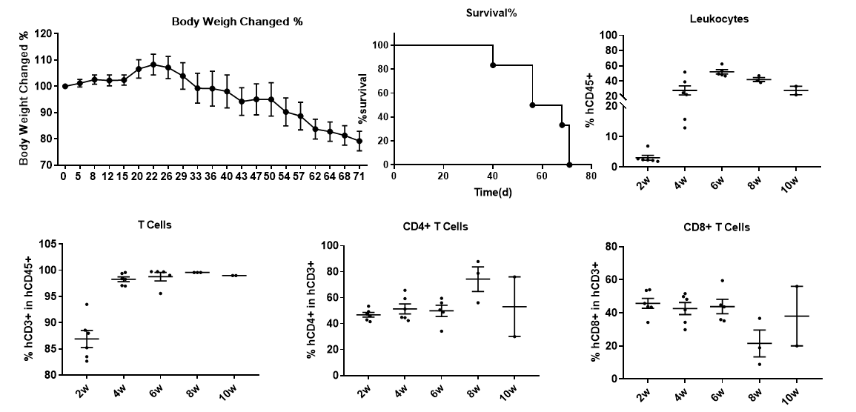
图19.FACS法分析外周血淋巴细胞亚群
将人PBMC细胞(5E6)静脉植入纯合子B-NDG小鼠(雌性,6周龄,n = 6)。植入huamn PBMC后不同时间取B-NDG小鼠血液进行流式细胞分析。B-NDG小鼠显示高百分比的人CD45 + 细胞,T细胞。B-NDG小鼠表现出体重减轻和生存期缩短,可能是由于高比例的人免疫细胞重建引起的GVHD效应。
利用PBMCs重建的B-NDG小鼠模型进行双特异性抗体药效评价
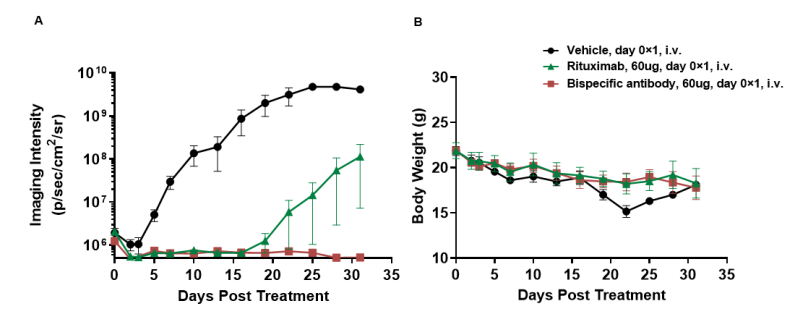
图 20 .使用 PBMC 细胞重建的 B-NDG 小鼠进行双特异性抗体药效研究
将人 B-luciferase-GFP Raji (5E5)、PBMC (5E6) 和抗体混合物静脉注射到 B-NDG 小鼠 (n = 4) 中。(A) 小动物成像仪监测小鼠肿瘤荧光。(B) 治疗期间的体重变化。单抗表现出明显的抑瘤效果,双特异性抗体的抑制作用更加显著。结果表明,使用 PBMC重建的B-NDG小鼠建立CDX肿瘤模型为体内评价抗体提供了有力的临床前模型。数值表示为平均值±SEM
人免疫系统重建模型和疗效评价
在使用人PBMC重建的B-NDG小鼠中评价双特异性抗体的体内药效
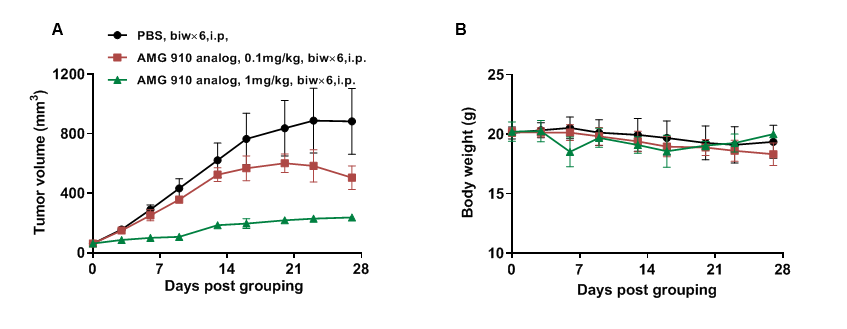
图20.使用PBMC细胞重建的B-NDG小鼠进行CD3×Claudin18.2双特异性抗体有效性研究。将人PBMC(5E6)静脉植入B-NDG小鼠(雌性,7周龄,n = 6)后,皮下植入NUGC4细胞(5E6)。当肿瘤大小约为50-80 mm3,人血液hCD45%百分比高于10%时,将动物分为对照组和给药组,此时给予药物处理。(A)抗人CD3×Claudin18.2双特异性抗体(AMG 910类似物)可抑制人PBMC重组B-NDG小鼠中的NUGC4肿瘤生长。(B)给药期间的体重变化。CD3×Claudin18.2双特异性抗体表现出明显的肿瘤抑制作用。结果表明,用重组PBMC建立B-NDG小鼠CDX肿瘤模型为抗体的体内评价提供了有力的临床前模型。数值表示为平均值±SEM。
利用B-NDG 小鼠成功建立HSC免疫重建模型
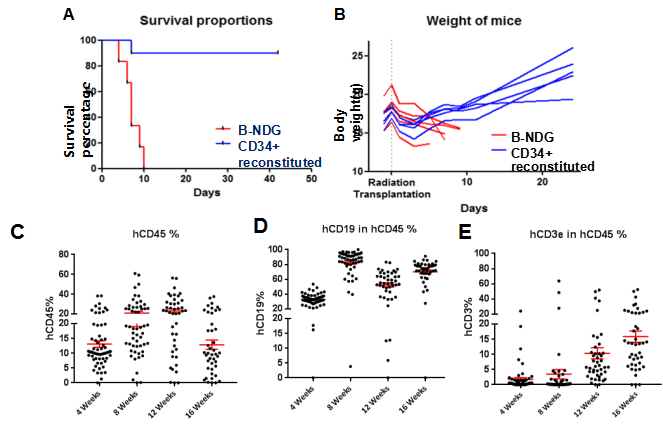
图21.利用人造血干细胞(CD34+)在B-NDG®小鼠体内重建免疫系统。
(A) 重建人 CD34 + 细胞可延长受辐照 B-NDG 小鼠的寿命;(B) B-NDG小鼠和 进行CD34+重建的 B-NDG 小鼠在辐照后的体重变化;(C)将 2 x 105 CD34+细胞植入 B-NDG 小鼠后,在不同的时间点连续测量人 CD45+细胞的百分比;(D) 人 CD45+细胞中人 CD19+ 细胞的百分比。(E) 人 CD3+ 细胞占人 CD45+ 细胞的百分比。结果表明利用B-NDG小鼠可以成功建立HSC人源化小鼠模型。
利用HSC免疫重建的 B-NDG 小鼠中进行的药物药效评价实验
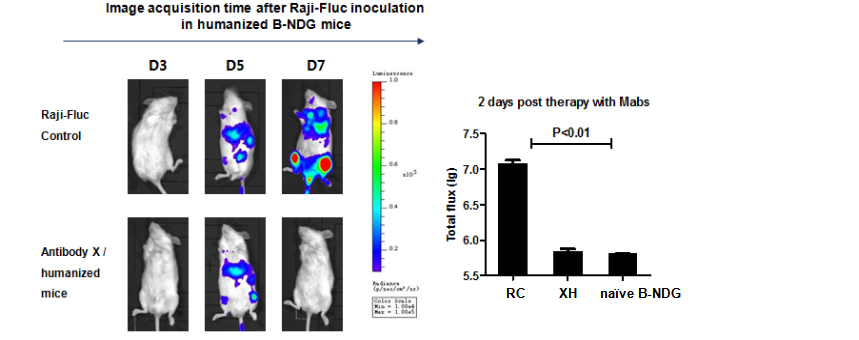
图 22.使用 CD34+ 细胞重建的 B-NDG小鼠模型进行药效评价
利用人CD34+细胞重建的人源化 B-NDG 小鼠模型静脉注射人B-luciferase-GFP Raji 细胞 (5E5)。肿瘤细胞植入后5天,用人抗体 X 处理小鼠。在第7天观察到人抗体X对肿瘤细胞生长的显著抑制作用。结果表明,基于B-NDG的HSC人源化小鼠模型为体内抗体评价提供了有力的临床前模型。数值表示为平均值±SEM。 RC:Raji-Fluc Control. XH: Antibody X/humanized mice. naïve B-NDG: B-NDG mice without Raji-Fluc and antibody treatment.











 京公网安备:
京公网安备: